De Wonderen van Water
Water heeft geen smaak, geen geur en geen kleur en voorziet ons niet van voedingsstoffen of energie. Toch is het essentieel voor leven op aarde. Maar, wat maakt water nou zo speciaal?
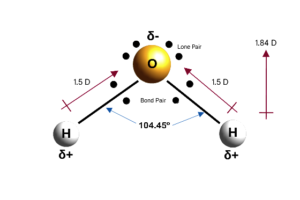
In het watermolecuul
Heb je ooit een fles water in de vriezer gedaan en vervolgens vergeten die eruit te halen? De volgende keer dat je de vriezer opende, zag je dat de fles gebarsten was. Maar waarom is dat? Voor de meeste substanties neemt de dichtheid toe wanneer ze afkoelen, wat betekent dat het volume vermindert. Echter, dit slaat niet op water, dat een maximale dichtheid heeft rond de 4° C. Boven en onder deze temperatuur neemt de dichtheid van water gestaag af, dit betekent dat water zich uitzet. Dit fenomeen wordt ook wel de anomalie van water genoemd. De reden waarom water zich zo ongebruikelijk gedraagt, komt door hun vermogen om waterstofbruggen te vormen. Dankzij deze verbinding, watermoleculen verzamelen zich in clusters, die al worden gevormd in de vloeibare staat. Bij 4°C zijn de clusters in het kleinst mogelijke volume geordend, zoals nette stapels in de schappen van een supermarkt. Echter als de temperatuur verder daalt, verandert de structuur als het kristalliseert, dit betekent dat het water opnieuw meer ruimte nodig heeft. Aan de andere kant, wanneer de temperatuur stijgt, zorgt de thermische beweging van de moleculen ervoor dat de clusters verdwijnen en water uitzet. Verder, laat het veel aquatische wezens in de winter overleven, omdat water van 4°C met de hoogste dichtheid naar de bodem zakt, wat ervoor zorgt dat het water daar vloeibaar blijft.
De anomalie van water
Heb je ooit een fles water in de vriezer gedaan en vervolgens vergeten die eruit te halen? De volgende keer dat je de vriezer opende, zag je dat de fles gebarsten was. Maar waarom is dat? Voor de meeste substanties neemt de dichtheid toe wanneer ze afkoelen, wat betekent dat het volume vermindert. Echter, dit slaat niet op water, dat een maximale dichtheid heeft rond de 4° C. Boven en onder deze temperatuur neemt de dichtheid van water gestaag af, dit betekent dat water zich uitzet. Dit fenomeen wordt ook wel de anomalie van water genoemd. De reden waarom water zich zo ongebruikelijk gedraagt, komt door hun vermogen om waterstofbruggen te vormen. Dankzij deze verbinding, watermoleculen verzamelen zich in clusters, die al worden gevormd in de vloeibare staat. Bij 4°C zijn de clusters in het kleinst mogelijke volume geordend, zoals nette stapels in de schappen van een supermarkt. Echter als de temperatuur verder daalt, verandert de structuur als het kristalliseert, dit betekent dat het water opnieuw meer ruimte nodig heeft. Aan de andere kant, wanneer de temperatuur stijgt, zorgt de thermische beweging van de moleculen ervoor dat de clusters verdwijnen en water uitzet. Verder, laat het veel aquatische wezens in de winter overleven, omdat water van 4°C met de hoogste dichtheid naar de bodem zakt, wat ervoor zorgt dat het water daar vloeibaar blijft.
Een blauwe planeet
Op aarde is er ongeveer 1,4 miljard kubieke kilometer water op aarde in totaal, wat water het meest verspreide molecuul op deze planeet maakt. Echter, het overgrote deel van de oceaan is zout water, die 3 kwart van het aardoppervlak bedekken. De oceanen geven de aarde haar blauwe kleur. Maar waarom blauw als water transparant lijkt te zijn? De reden: water absorbeert licht tussen 600 tot 800 nanometer. Dit is de lange golflengte van zichtbaar licht, oftewel, de kleur rood. Korte licht golflengtes, aan de andere kant, wat mensen waarnemen als blauw, worden niet geabsorbeerd door water, maar verstrooid. Dit geeft de impressie dat de kleur van water blauw is. Ondanks de kleur van onze planeet suggereert dat er meer dan genoeg water is, alleen is maar 3% van het water, zoet water en daarmee drinkbaar. Echter, twee derde van dat zoete water zit vast in de ijskappen en gletsjer en dus niet beschikbaar voor ons. Een ander groot deel van het zoete water wordt gevonden als grondwater en een klein percentage is dus in rivieren en meren van onze planeet. Zodoende heeft de aarde een ongelofelijke hoeveelheid water die onze planeet een blauwe kleur geeft, zoet water daarentegen is een eindige bron en moet verantwoordelijk gebruikt worden.

Het element van leven
Water wordt niet voor niets het element van het leven genoemd. Het volbrengt veel taken in ons lichaam en functioneert onder veel verschillende namen. Als voorbeeld, ons brein drijft rond in wat ook wel bekend staat als hersenvocht, wat het brein beschermt tegen schokken en zorgt voor transport tussen de cellen. Voor het behouden van de druk in onze ogen hebben we het glasachtige lichaam - een vloeistof dat voornamelijk bestaat als water. We zijn ook afhankelijk van water voor onze ademhaling, onze longen moeten vochtig zijn voor een optimale uitwisseling van zuurstof en koolstofdioxide. Niet te vergeten ons cardiovasculaire systeem, dat bloed distribueert dus water, door ons hele lichaam. Door de moleculaire eigenschappen, water functioneert in ons lichaam als medium, oplosmiddel en katalysator. Bijvoorbeeld, zouten zijn essentieel voor ons voortbestaan en zijn opgelost in ons lichaamsvloeistoffen als ionen, veel chemische reacties hebben water nodig om plaats te vinden. Vergeleken met andere vloeistoffen, kan water ook relatief veel energie opnemen zonder significant op te warmen. Dit bekent dat het te veel aan energie van chemische reacties in onze cellen geabsorbeerd kan worden door water, daarmee wordt het oververhitten van de cel voorkomen.
Ook al ziet het kleine molecuul er schijnbaar eenvoudig uit in het eerste opzicht, water vormt ons lichaam evenals zowel onze planeet. Het speelt een significante rol die functioneert in de kleinste cel tot hele ecosystemen en de reden waarom er überhaupt leven mogelijk is.
Bron
Triebskorn, R., and Wertheimer, J. (2016). Wasser als Quelle des Lebens: Eine multidisziplinäre Annäherung. 10.1007/978-3-662-46268-3






0 Reacties
Geef een reactie